Klīniskais gadījums: subkardijas polips no atklāšanas līdz polipektomijai
Subkardijas polips ir audu veidojums, kas attīstās kuņģa gļotādas iekšējā slānī, precīzāk, kuņģa kardijas daļā. Termins “subkardija” būtībā apraksta polipa atrašanās vietu, nevis tā šūnu tipu. Polips var būt labdabīgs, taču atkarībā no tā veida un lieluma tam var būt potenciāls kļūt par ļaundabīgu. Tāpēc ļoti svarīgi ir veikt papildu izmeklējumus, lai noteiktu precīzu polipa dabu.
Ar šo klīnisko gadījumu 2025. gada 16. jūlijā GASTRO CENTRA ārstu konsīliju iepazīstināja Krista Cēbere-Kristone, ārste rezidente gastroenteroloģijas specialitātē.
Paciente, 64 gadus veca sieviete, vērsās pie ārsta ar atviļņa simptomiem un sūdzībām par dedzināšanu.
2024. gada oktobrī pacientei veica EGDS, kuras laikā barības vada distālajā daļā tika atrasts polips. Histoloģiskā atbilde apstiprināja barības vada plakanšūnu papilomu. Pacientei tika diagnosticēta H. pylori infekcija, par ko viņa saņēma eradikācijas terapiju. Ikdienā lietot medikamenti omeprazols, metoprolols un izmantota antihipertensīvā terapija (Perindoprilum/Amlodipinum).
Laboratoriskajās analīzēs 2024. gada septembrī hemoglobīna līmenis bija normāls, tā paša gada novembrī vēdera dobuma USG uzrādīja hepato un aizkuņģa dziedzera steatozi, kā arī angiomiolipomu labajā nierē.
Krista Cēbere-Kristone
Pacientei atviļņa simptomi dinamikā saglabājās, tāpēc pati iniciēja atkārtotu augšējās endoskopijas izmeklēšanu.
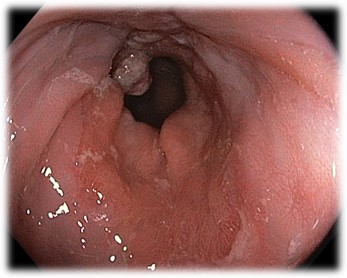
Šī gada 19. jūnijā veiktajā augšējā endoskopiskajā izmeklēšanā bija redzams, ka kuņģis, divpadsmitpirkstu zarna un pārējās augšējā gremošanas trakta daļas ir normālas: gļotāda kuņģī ir ar akcentētu sīko asinsvadu zīmējumu, tomēr bez redzamiem bojājumiem, kuņģa krokas visās tā daļās ir elastīgas, regulāras un, iestiepjot ar gaisu, izlīdzinās, kas liecina par normālu sieniņas funkcionalitāti, piloriskais kanāls ir brīvi caurejams, divpadsmitpirkstu zarnas bulbārās daļas gļotāda ir bez redzamiem bojājumiem, pāreja uz descendējošo daļu nav traucēta, gļotādai ir normāls krokojums, taču distālajā daļā bija redzama epitelizēta erozija, kas garumā pārsniedz 5 mm. Tieši zem kardijas līnijas tika atrasts 10 mm liels polipoīds veidojums ar papillomatozu virsmas struktūru, ap kuru bija vizuāli hiperplastiski audi. Tika paņemtas šī veidojuma un apkārtējās gļotādas biopsijas.
Augšējā endoskopija 19.06.2025.
Barības vada distālā daļa maisveidīgi ieslīd virs diafragmas atveres.
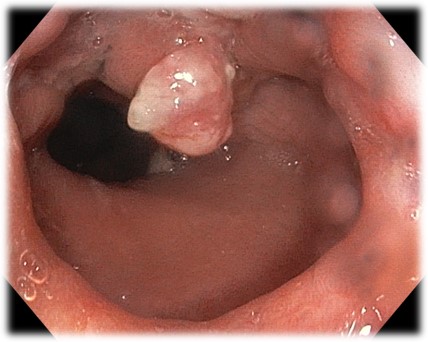
Subkardijas polips saistībā ar diafragmas trūci.
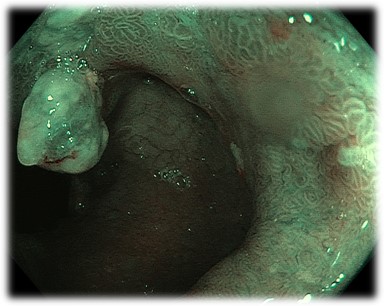
Subkardijas polips šaurjoslas (NBI) gaismā.
Endoskopijas slēdziens norādīja uz subkardijas polipoīdu (10 mm), “B” pakāpes ezofagītu un hiatālas trūces ainu, savukārt biopsijas materiāla izmeklēšana no subkardijas zonas polipa un izmainītās gļotādas ap to norādīja uz subkardijas hiperplastisku polipu. H. pylori tests bija negatīvs.
Atkārtota EGDS + EUS laikā tika paņemtas mērķētas biopsijas; EUS apraksta vienmērīgu, plānu, hipoehogēnu muskuļslāni bez invāzijas pazīmēm. Histoloģija: provizoriski – hiperplastiska morfoloģija, bet gala vārds pēc pilnīgas polipektomijas materiāla izvērtēšanas.
Histoloģiskais slēdziens.
Hiperplastisks polips ir biežākais šāds atradums subkardijas zonā. Kopumā šie polipi ir labdabīgi, tomēr >10 mm veidojumiem displāzijas risks pieaug, tāpēc, lai neriskētu un iegūtu pilnu histoloģiju, polips tika noņemts. Vienlaikus sakārtots arī fons – novērtēts H. pylori un, ja ir pozitīvs, tas jāizārstē, jo tā var mazināt polipu veidošanos un recidīvus. Refluksa kontrole (PSI + dzīvesveids) palīdzēs dziedēt ezofagītu un mazināt simptomus.
Septembrī pacientei plānveidā tiks veikta polipektomija.
Hiperplastiskie polipi bieži rodas hroniska gastrīta vai H. pylori infekcijas rezultātā, un tiem ir zems ļaundabīgās transformācijas risks. Tomēr lielākiem polipiem (>10 mm) ir nedaudz lielāks displāzijas potenciāls.
- Eiropas Kuņģa un zarnu trakta endoskopijas biedrība (ESGE) iesaka veikt biopsijas vai rezekciju hiperplastiskiem polipiem, kas ir lielāki par 10 mm.
- Amerikas Gastroenteroloģijas koledža rekomendē visiem hiperplastiskiem polipiem, kas lielāki par 10 mm, veikt pilnīgu polipektomiju un ņemt biopsijas no neskartās gļotādas.
- Lieliem hiperplastiskiem polipiem pastāv liels recidīva risks (līdz 55 %) pēc noņemšanas.
Kuņģa polipu veidi – endoskopiskās un histoloģiskās iezīmes
| Polipa tips | Neoplastiskais potenciāls | Lokalizācija | Sākotnējā vadība | Tālākā novērošana |
| Fundālo dziedzeru polips (sporādisks vai FAP) | Zems | Sporādisks: kuņģa korpuss, fundus
FAP: viss kuņģis |
Biopsija, ja <1 cm;
Ja >1cm, apsvērt polipektomiju |
Ja nav displāzijas: nav nepieciešama novērošana
Ja ir displāzija: apsvērt FAP un veikt kolonoskopiju. |
| Hiperplastisks polips. | Minimāls (bet varbūt sinhroni audzēji) | Jebkura kuņģa daļa | Biopsija vai polipektomija
Biopsijas arī starp polipiem Testēt/ārstēt H. pylori |
EGDS es pēc 1 gada
Ja polips saglabājas vai ir displāzija, polipektomija un atkārtots EGDS Ja nav displāzijas, kontrole nav nepieciešama |
| Adenomatozs polips | Augsts | Jebkura kuņģa daļa | Pilnīga polipektomija
Biopsijas apkārtējā gļotādā Izmeklēt visu kuņģi |
Nepilnīga izņemšana vai augstas pakāpes displāzija:
kontrole pēc 6 mēnešiem Pilnīga izņemšana bez displāzijas: kontrole pēc 1 gada |
| Iekaisīgs fibrozs polips | Ļoti zems | Antrums vai prepilors | Biopsija
Noņemt, ja izraisa obstrukciju |
Nav nepieciešama novērošana |
| Kuņģa neiroendokrīnais audzējs | Atkarīgs no veida | Jebkura daļa
I/II: Fundus/ķermenis (klastras): jebkur, solitārs |
Biopsija vai endoskopiska izņemšana (ja <1 cm un 3-5 gab., I tips)
Biopsijas no plakanas gļotādas |
I tips: nav kontroles, ja pilnībā izņemts; Saistīts ar AMAG. II: jāizvērtē gastronoma/MEN1
III/UV: pārbaudīt metastāzes, apsvērt operāciju |
| Ektopiska aizkuņģa dziedzera audi | Nav | Submukozs veidojums ar centrālu iedobi | Biopsija ja ir neskaidrība | Nav nepieciešama novērošana |
| GIST (gastrointestināls stromāls audzējs) | Augsts | Submukozs mezglus ar centrāli čūlu. | Biopsija vai FNA ar EUS palīdzību | Strīdīgi – ja netiek izņemts, var sekot ar EUS |
| Leiomioma | Zems | Apaļš, submukozs elastīgs audzējs | Biopsija vai FNA ar EUS | Nav nepieciešama novērošana, ja nav simptomu |
Literatūra:
- Pimentel‑Nunes P, Libânio D, Lage J, Esposito G, Garrido M, et al. Management of epithelial precancerous conditions and lesions in the stomach (MAPS II). ESGE Guideline. Endoscopy. 2019;51(4):365–388. doi:10.1055/a‑0859‑1883.
- Carmack SW, Genta RM, Schuler CM, Saboorian MH. The current spectrum of gastric polyps: correlation with Helicobacter pylori infection and gastric atrophy. Am J Gastroenterol. 2009;104(6):1524–1532. doi:10.1038/ajg.2009.139.
- Islam RS, Patel NC, Lam‑Himlin D, Nguyen CC. Gastric polyps: a review of clinical, endoscopic, and histopathologic features and management decisions. Gastroenterol Hepatol (N Y). 2013;9(10):640–651.
- Orłowska J, Jarosz D, Pachlewski J, Butruk E. Malignant transformation of gastric hyperplastic polyps. Am J Gastroenterol. 1995;90(12):2152–2159.
- Ahn JY, Son DH, Choi KD, et al. Effect of Helicobacter pylori eradication on gastric hyperplastic polyps: a prospective analysis. Endoscopy. 2011;43(12):1076–1082. doi:10.1055/s‑0030‑1256677.
- Park DY, Lauwers GY. Gastric polyps: classification and management. Arch Pathol Lab Med. 2008;132(4):633–640.
- Sonnenberg A, Genta RM. Prevalence of benign gastric polyps in a large pathology database. Dig Liver Dis. 2015;47(2):164–169.